Sắt là kim loại khá phổ biến trong vỏ quả đất. Sắt nguyên chất kỹ thuật có cơ tính như sau:
HB ≈ 80; σb ≈ 250MPa; σ0,2 ≈ 120MPa;
δ ≈ 50%; Ψ ≈ 85%; aK ≈ 2500kJ/m2
Xem thêm: Chuyển biến khi làm nguội chậm trong vật liệu
So với các kim loại khác (nhôm, đồng) nó cũng khá dẻo (dễ biến dạng nguội), dai, tuy bền, cứng hơn nhiều song vẫn còn rất thấp so với yêu cầu sử dụng.
Khi đưa cacbon vào sắt, giữa hai nguyên tố này xảy ra cả hai tương tác (hòa tan thành dung dịch rắn và tạo nên pha trung gian), đều có tác dụng hóa bền, nhờ đó hợp kim Fe – C trở nên bền cứng hơn (sắt) và đang được sử dụng một cách rộng rãi nhất.
Tương tác hóa học giữa Fe và C
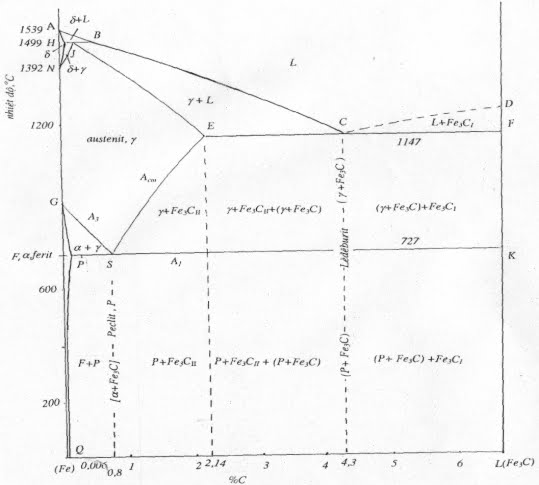
Khi lượng cacbon đưa vào sắt vượt quá giới hạn hòa tan (phụ thuộc vào dạng thù hình và nhiệt độ), sau khi đi vào các lỗ hổng để tạo nên dung dịch rắn xen kẽ, các nguyên tử cacbon thừa ra sẽ kết hợp với sắt thành Fe3C gọi là xêmentit.
Như đã biết đó là pha xen kẽ với kiểu mạng phức tạp, có thành phần 6,67%C + 93,33%Fe.
Thực ra còn có grafit là pha ổn định hơn xêmentit, tuy nhiên trong hợp kim thuần Fe – C sự tạo thành grafit là rất khó khăn nếu không muốn nói là không thể được, vì vậy xêmentit là pha giả ổn định và được coi là ổn định.
Trong thực tế sự tạo thành grafit có thể dễ dàng hơn nhiều khi có các yếu tố thuận lợi về thành phần và tốc độ nguội.
Cập nhật lúc 20:06 – 29/09/2019
